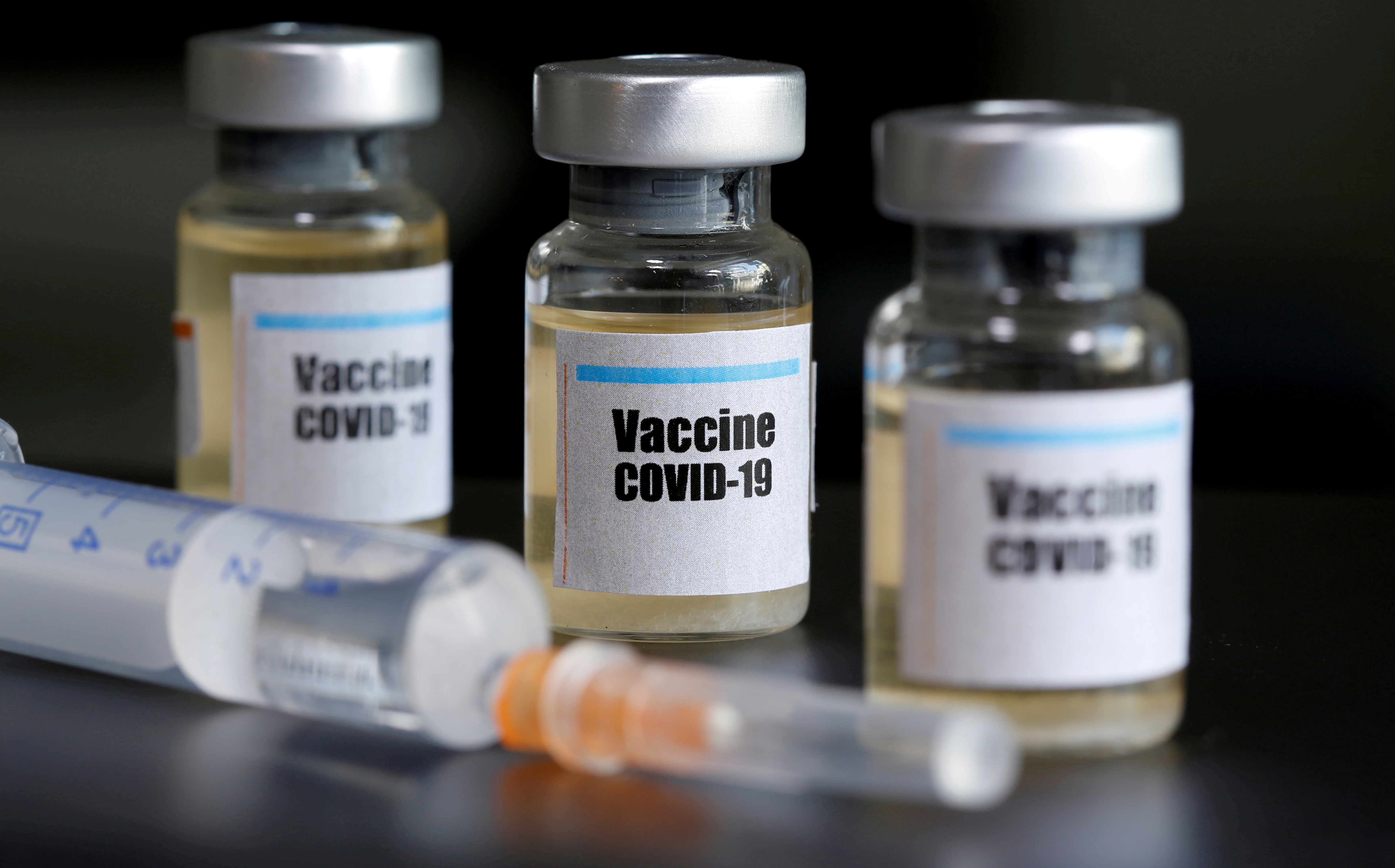
Две недели назад в Великобритании после шестидневного перерыва заново запустили проверку одной из лидирующих вакцин, разработанной Оксфордским университетом и фармацевтической компанией AstraZeneca. Во время перерыва специалисты проверяли безопасность вакцины. Также были возобновлены эксперименты в Южной Африке и Бразилии, но Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) пока не дает зеленого света американским исследованиям. Спонсоры британского исследования пока что скудно делятся информацией о том, чем была вызвана пауза и почему испытаниям позволили возобновиться. Некоторые ученые предполагают, что нехватка прозрачности может подорвать доверие общественности к вакцине.
Вдобавок растут опасения, что в дело вмешается политика и вакцину одобрят для срочного применения без достаточных доказательств ее эффективности. Президент США Дональд Трамп заявил, что хочет получить вакцину еще до президентских выборов в ноябре.Чтобы отвести подозрения, фармацевтические компании, стоящие за тремя ведущими вакцинами от коронавируса, находящимися на третьей стадии испытаний, — AstraZeneca, Pfizer и Moderna — на прошлой неделе опубликовали информацию о том, как проходят испытания.
Протоколы этих испытаний включают стандарты безопасности и успешности, а также некоторую неизвестную ранее информацию, например, о том, как скоро могут стать известны предварительные результаты исследований. В этих материалах также указано, что компании могут прекратить испытания на ранних этапах, если получат разрешение на выпуск в ускоренном порядке.
Вот три вопроса, связанных с текущими испытаниями вакцин, которые особенно волнуют ученых.
Безопасность и прозрачность
Изначально исследователей не очень волновали сообщения СМИ о том, что запись на испытания оксфордской вакцины была приостановлена 6 сентября из-за неблагоприятной реакции одного из участников. Неблагоприятные реакции — распространенное явление во время клинических испытаний, и зачастую они не связаны с предметом исследования. Некоторые специалисты предполагают, что, возможно, так и было в случае с оксфордской вакциной, учитывая, как быстро британские надзорные органы позволили возобновить испытания. В некоторых изданиях сообщили, что у участника развился поперечный миелит, то есть воспаление спинного мозга, но AstraZeneca и Оксфорд, спонсоры британского испытания, не поделились информацией о состоянии здоровья этого человека.
Некоторые исследователи раскритиковали непрозрачность в подаче информации, особенно когда выяснилось, что это уже второй перерыв в испытаниях из-за неблагоприятной реакции. В информационных листах, которые выдали участникам в июле, было сказано, что испытания уже останавливали, потому что у одного человека развился, предположительно, поперечный миелит. Затем, по утверждению компании AstraZeneca, этому пациенту поставили диагноз рассеянный склероз, и независимый консилиум определил, что это состояние не было связано с вакциной. Но компания и Оксфорд так и не сказали, получали ли эти два участника вакцину или плацебо.
Если выяснится, что у двух людей развился поперечный миелит, учитывая сравнительно небольшое число привитых людей, это будет весомо, считает Райна Макинтайр, эпидемиолог Университета Нового Южного Уэльса в Сиднее, Австралия. «Если произойдет еще один такой случай, испытания будет уже очень сложно восстановить», — говорит эксперт.
Макинтайр отмечает, что вирусные инфекции связывают как с поперечным миелитом, так и с рассеянным склерозом. Случаи поперечного миелита также наблюдали у людей с COVID-19, говорит она. Чтобы убедиться, что вакцина не связана с этим заболеванием, исследователи должны провести статистический анализ и сравнить вероятность возникновения такого состояния у участников, которые получили вакцины, с вероятностью их возникновения у тех людей, которые получили плацебо. «Вот почему, наверное, FDA, все еще не определилось, разрешить ли продолжить испытания в США», - говорит Макинтайр.

«Необходимо опубликовать больше информации о том, почему испытания были приостановлены и потом возобновлены», — считает Хильда Бастиан, которая преподает доказательную медицину в Университете Бонда (Голд-Кост, Австралия). Недостаточная прозрачность со стороны спонсоров испытаний вызывает озабоченность и может привести к тому, что некоторые участники покинут исследование либо люди не захотят делать прививку, когда вакцину одобрят, говорит Бастиан. «Нам крайне необходимо, чтобы люди доверяли вакцинам, которые так быстро создаются», — подчеркивает специалист.
AstraZeneca и Оксфорд не ответили на призыв к большей прозрачности. Но исполнительный директор AstraZeneca, Паскаль Сорио, заявил во время панельной дискуссии, устроенной Мировым экономическим форумом 24 сентября, что руководства по клиническим испытаниям рекомендуют не раскрывать информацию об отдельных участниках, дабы избежать нарушения конфиденциальности и профессиональной этики.
Сорио также рассказал, что, учитывая интерес общественности к вакцинам, компании обсуждают, насколько они могут поделиться информацией, не нарушая хода испытаний.
Роль политики
Доверие общества к вакцинам от коронавируса уже колеблется, в частности в Соединенных штатах, где Трамп регулярно расхваливает свою программу Operation Warp Speed (Операция «Сверхсветовая скорость»), цель которой — форсировать разработку вакцины от COVID-19. На фоне риторики Трампа Исследовательский центр Пью в Вашингтоне 17 сентября сообщил, что, согласно опросам общественного мнения, доля взрослых людей в США, согласных сделать прививку от COVID-19, упала с 72 % в мае до 51 % в сентябре. Три четверти опрошенных в сентябре верили, что в США одобрят вакцину до того, как будет точно известно о ее безопасности и эффективности.
Речь идет не об антипрививочниках. Даже исследователи, участвующие в разработке вакцин и их испытаниях, беспокоятся, что на процесс регистрации вакцины могут повлиять политические, а не научные соображения. «Я проверю данные о безопасности, прежде чем сделаю уколы моим детям», — говорит Курт Вайль, директор моделирования и симуляции в Berry Consultants, консалтинговой компании в области организации клинических испытаний.
Недоверие заметно не только в Соединенных штатах. В Европе переговоры о поставках вакцин, которые компании ведут за закрытыми дверями, также подливают масла в огонь, — рассказывает Яннис Натсис, менеджер по политике правозащитной группы European Public Health Alliance в Брюсселе. «Мы не хотим дурно отзываться о вакцинах, мы хотим укрепить доверие к ним, — объясняет он. — Но информации не хватает катастрофически».
В США путь к ускоренному выпуску критически важных медицинских средств открывает экстренное разрешение на применение (EUA), которое выдает FDA. И оно является одной из причин недоверия. EUA позволяет обойти обычную процедуру регистрации и приступить к использованию медицинских препаратов, если они «могут быть эффективны». «Учитывая расплывчатость и непрозрачность, оно потенциально подвержено влиянию политических сил», — говорит Гершель Начлис, который занимается исследованием политики в области здравоохранения в Дартмутском колледже Хановера (Нью-Гэмпшир).
Ранее в двух случаях выдача EUA потенциальным лекарствам от COVID-19 уже вызывали подозрения в политическом вмешательстве. Речь идет о средстве от малярии гидроксихлорохине и переливаниях плазмы крови людей, переболевших коронавирусом. Трамп высказывался в пользу обоих средств, и ни за одним из них не стояло крупного рандомизированного двойного слепого испытания — золотого стандарта клинических испытаний. EUA по гидроксихлорохину отозвали, когда клинические данные показали, что он неэффективен для людей, госпитализированных с COVID-19. EUA для плазмы крови объявили за день до крупного съезда, который проводила партия Трампа.
Так что, когда на прошлой неделе компании опубликовали протоколы клинических испытаний трех ведущих вакцин, исследователи сосредоточились на деталях. «В целом протоколы выглядели сравнительно нормальными», — говорит Дэвид Бенкесер, специалист по медико-санитарной статистике Университета Эмори в Атланте. «Но одна вещь бросалась в глаза», — добавляет Бенкесер. По протоколу Pfizer, внешним экспертам, назначенным для мониторинга безопасности испытаний, разрешено изучать промежуточную информацию чаще, чем по протоколам двух других компаний. Это значит, что первый анализ результатов можно будет провести уже после того, как исследователи соберут информацию всего о 32 зараженных подопытных, с учетом тех, кому дали и вакцину, и плацебо. Этого этапа можно достичь всего за три месяца с начала испытаний в июле — практически перед выборами в США.
Если анализ на раннем этапе покажет, что вакцина эффективно сократила инфицирование в этой маленькой выборки, испытания могут остановить и компания может подать заявку на EUA. «Доказать, что вакцина достаточно хорошо работает, чтобы отвечать стандартам EUA, на этой ранней стадии можно, но это не позволит провести долгосрочного наблюдения, чтобы убедиться в ее безопасности», — говорит Вайль. «Трех месяцев также слишком мало, чтобы достаточно разобраться в том, насколько долго сохраняется иммунитет после прививки», — отмечает он. Pfizer не ответили, почему они организовали свои клинические испытания таким образом и планируют ли продолжить отслеживать безопасность вакцины, если испытания прекратятся преждевременно.
«Критически важно, чтобы компания продолжала собирать данные о безопасности, даже если испытания закончатся быстро, и сделала эту информацию доступной, чтобы успокоить взволнованную общественность», — говорит Вайль.
По слухам, FDA планирует усовершенствовать механизм EUA для вакцин от COVID-19. Судя по статье, опубликованной 22 сентября в The Washington Post, Управление будет требовать сбора данных практически на уровне стандартного испытания. FDA отказалось прокомментировать эту информацию, а Трамп заявил, что он может блокировать такие меры.
Начлис также отмечает, что внешний консультативный совет FDA, скорее всего, будет обсуждать вакцину на публичных слушаниях, что сделает решение более прозрачным, чем предыдущие решения по выдаче EUA. «Нам нужно повысить уровень стандартов и прозрачности, — говорит он. — И я думаю, в этом направлении уже есть существенное движение».
Цели и эффективность вакцин
Даже если надзорные органы одобрят три ведущие вакцины, исследователи предупреждают, что уколы могут не дать людям того, на что они надеются.
Протоколы AstraZeneca, Pfizer и Moderna показали, что испытания рассчитаны на проверку способности вакцины предупреждать клинические проявления COVID-19, а не его тяжелое течение, которое требует госпитализации и может привести к смерти.
Макинтайр и другие исследователи считают, что было бы лучше проверить, способны ли вакцины предотвратить тяжкое заболевание и смерть. «Если укол может существенно сократить риск серьезных осложнений, тогда вирус будет действовать на привитых людей так же, как обычная простуда», — говорит она.
В текущей третьей фазе испытаний каждого средства участвуют несколько десятков тысяч участников. «Но для испытания, которое могло бы показать, насколько вакцина сокращает риск тяжелого течения COVID-19, требуется больше подопытных и больше времени», — объясняет Томас Ламли, специалист по медико-санитарной статистике Оклендского университета, Новая Зеландия. «Нынешние испытания пошли по среднему пути между определением, предотвращают ли вакцины любое инфицирование вирусом и предотвращают ли они развитие тяжелого хода болезни», — говорит он.
Цель компаний — добиться того, чтобы как минимум 50 % привитых людей не заболели клинической формой COVID-19. Это определение успешности согласно руководству FDA. При этом создатели надеются на эффективность в 60 % и выше.
Но даже 60 % будет мало для развития коллективного иммунитета, при котором предотвращается распространение заболевания, говорит Ламли. «Чтобы достичь этой цели, вакцина должны быть как минимум на 80 % эффективна, учитывая тот факт, что не все люди ее получат», — объясняет Макинтайр. «Тем не менее вакцинирование большой доли населения одной из этих прививок значительно облегчит контроль над распространением вируса, если сочетать его с другими мерами, такими как ношение масок и отслеживание контактов, — считает Ламли. — Даже умеренно эффективная вакцина станет огромной подмогой».